Caso del mes Junio 2017
« Todos los casos
Caso del mes Junio 2017
Descripción
Autores
- Dra. Catherine Facenda Pérez. Radiodiagnóstico, Lleida, Hospital Universitario Arnau de Vilanova, [email protected].
- Dr. Robert Beguè Gomez. Radiodiagnóstico, Institut de Diagnòstic per la Imatge (IDI), Lleida, [email protected]
- Dra. Anna Abu-Suboh Abadia. Radiodiagnóstico, Hospital Santa María, Lleida, [email protected]
Historia Clínica
-
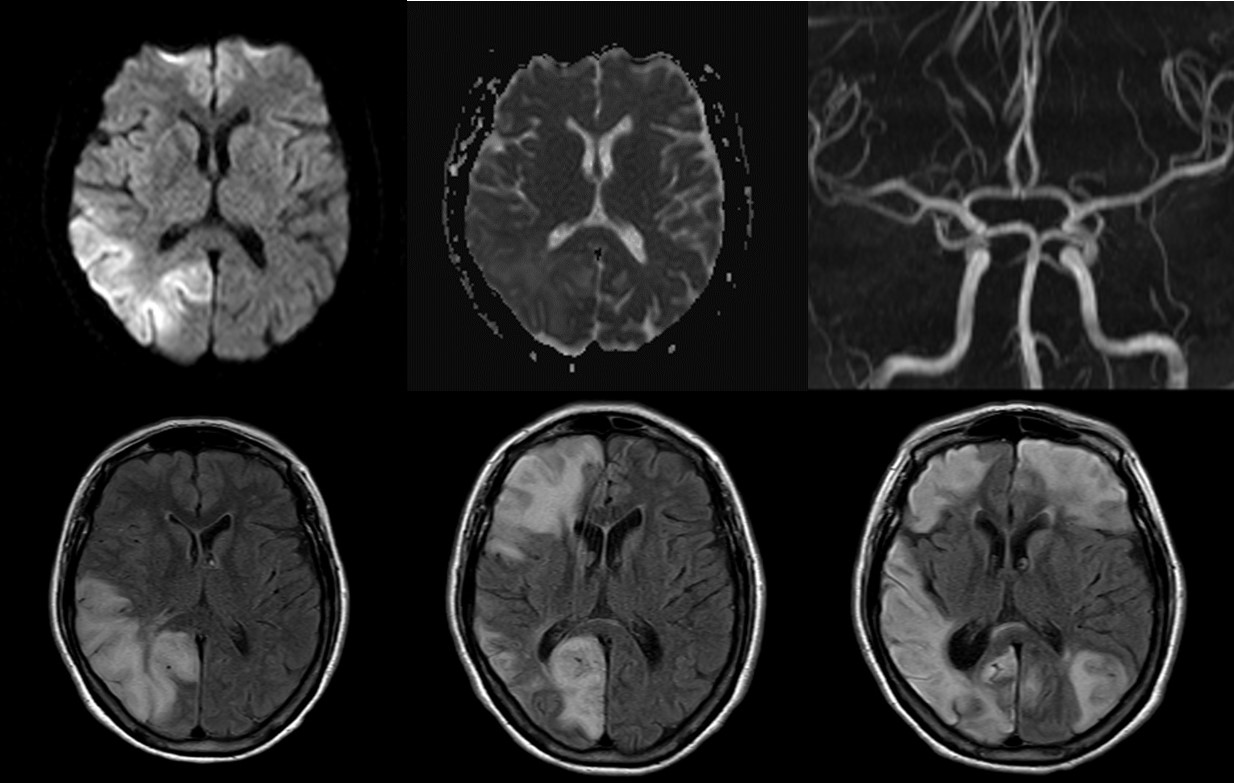
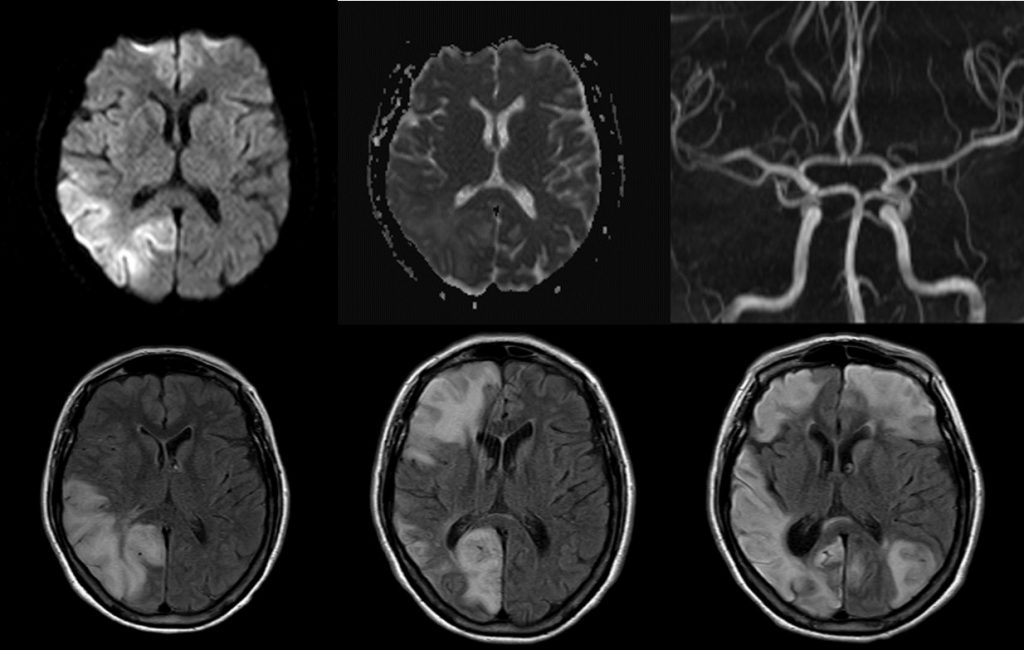
Mujer de 40 años con diagnóstico de carcinoma de endometrio y de mama en tratamiento que presenta ataques de migraña occipital y ataxia.
Leyendas

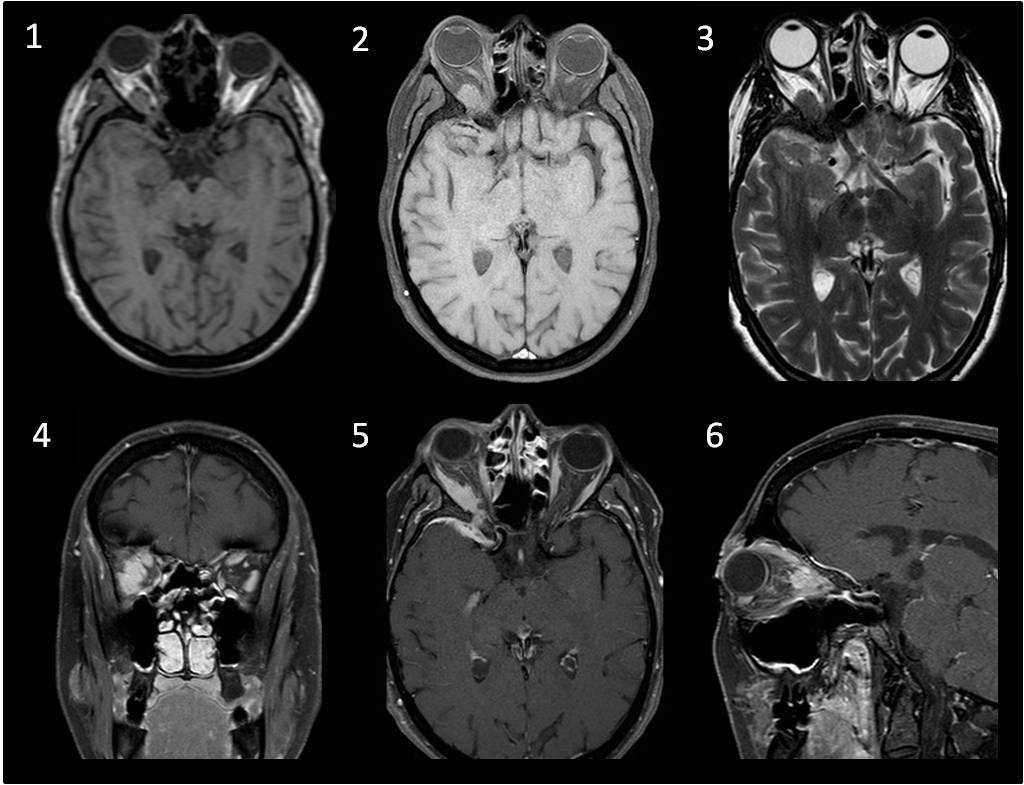
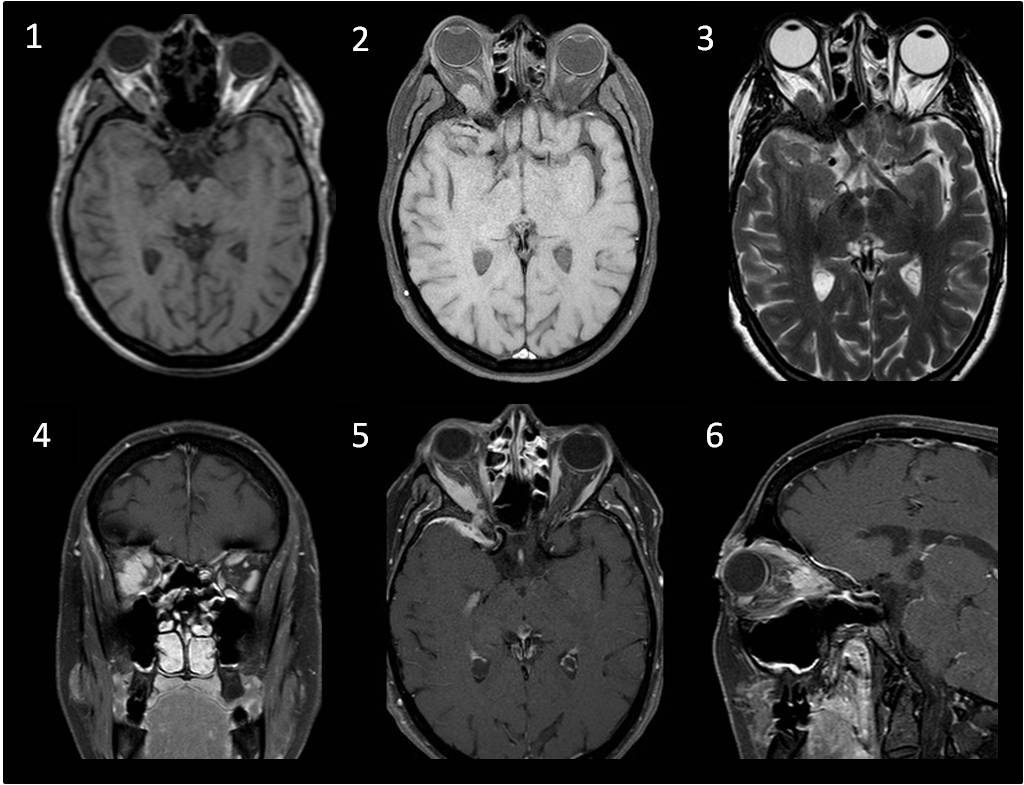
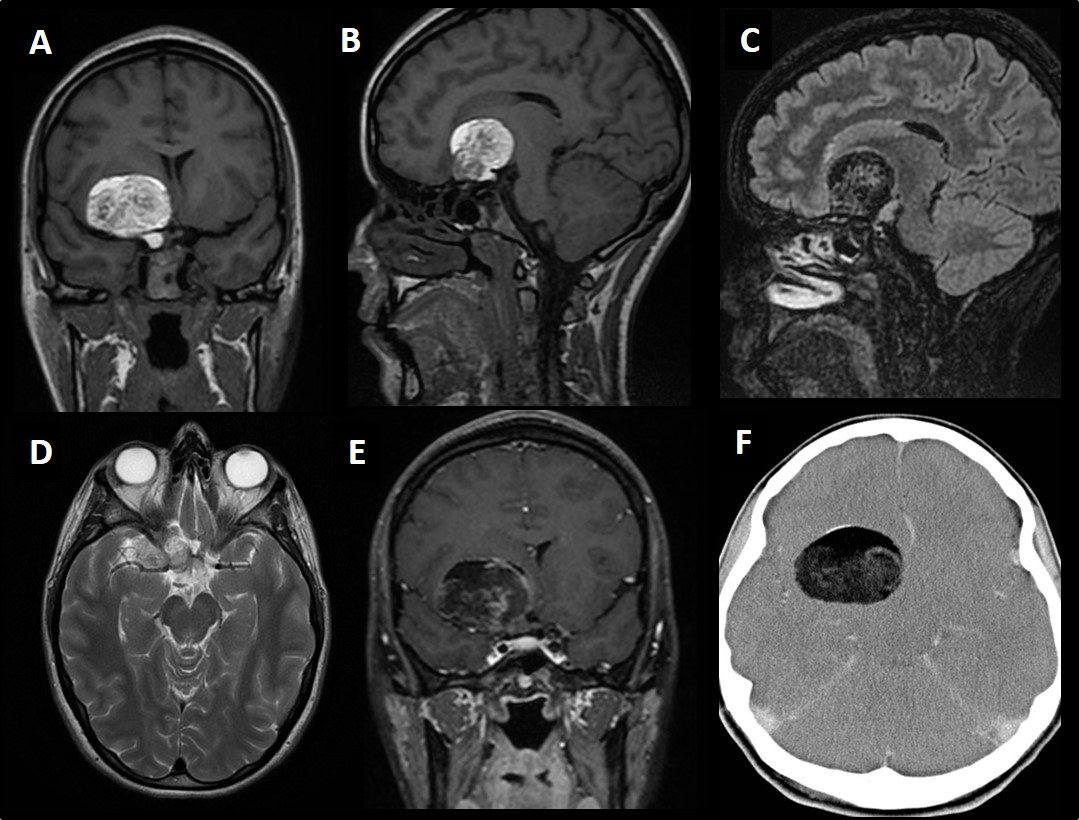
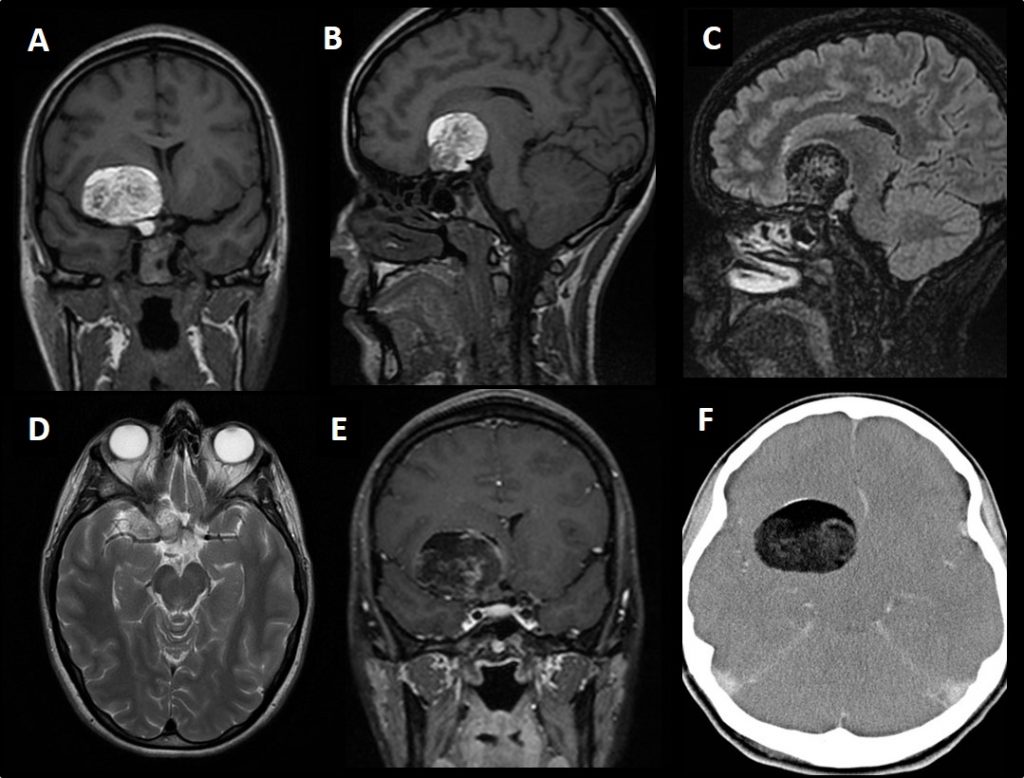
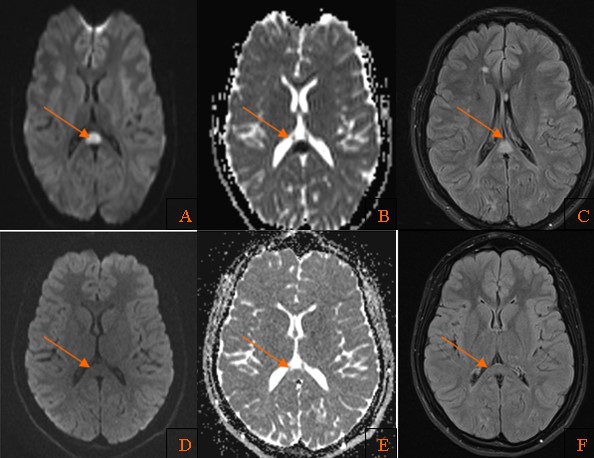
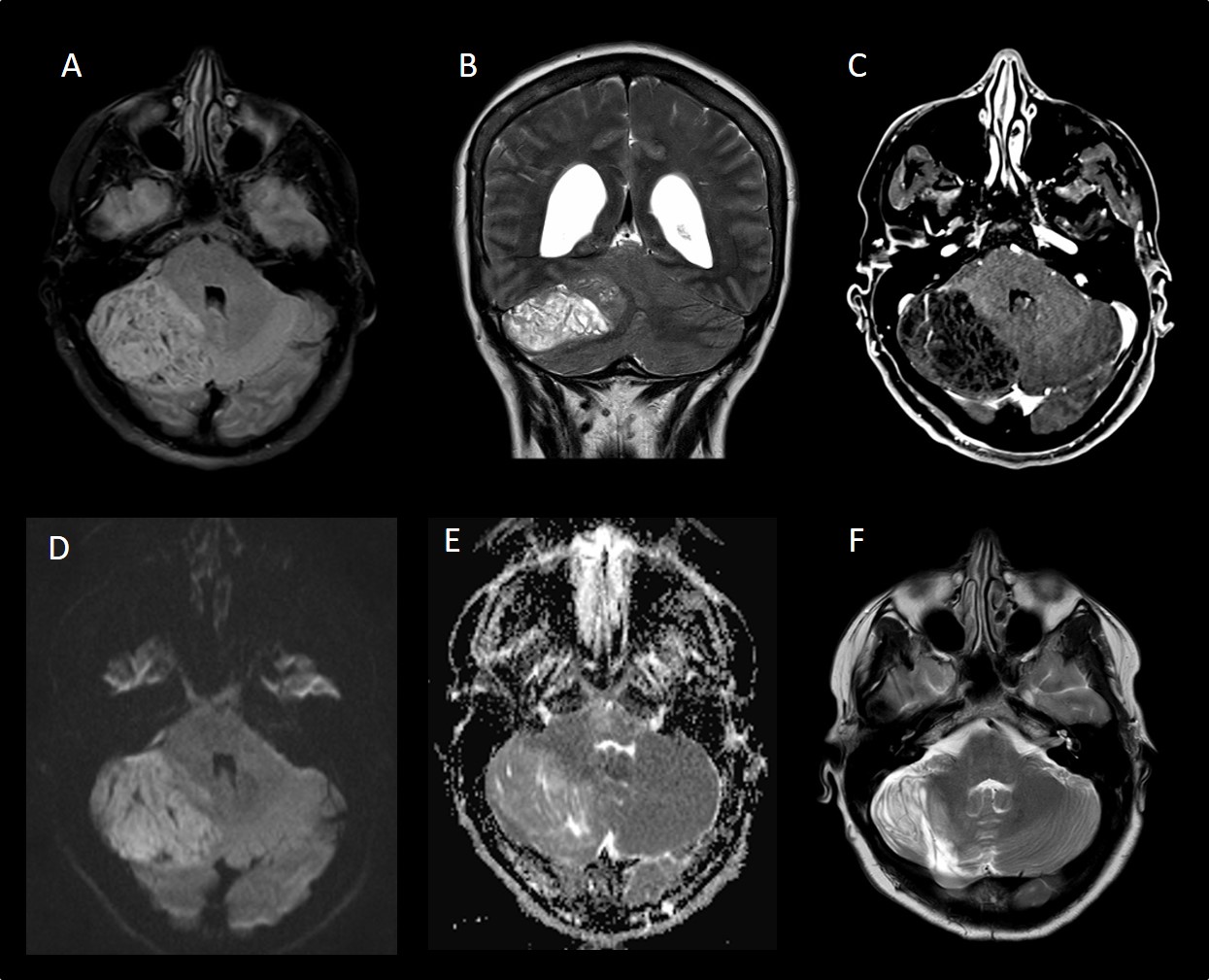
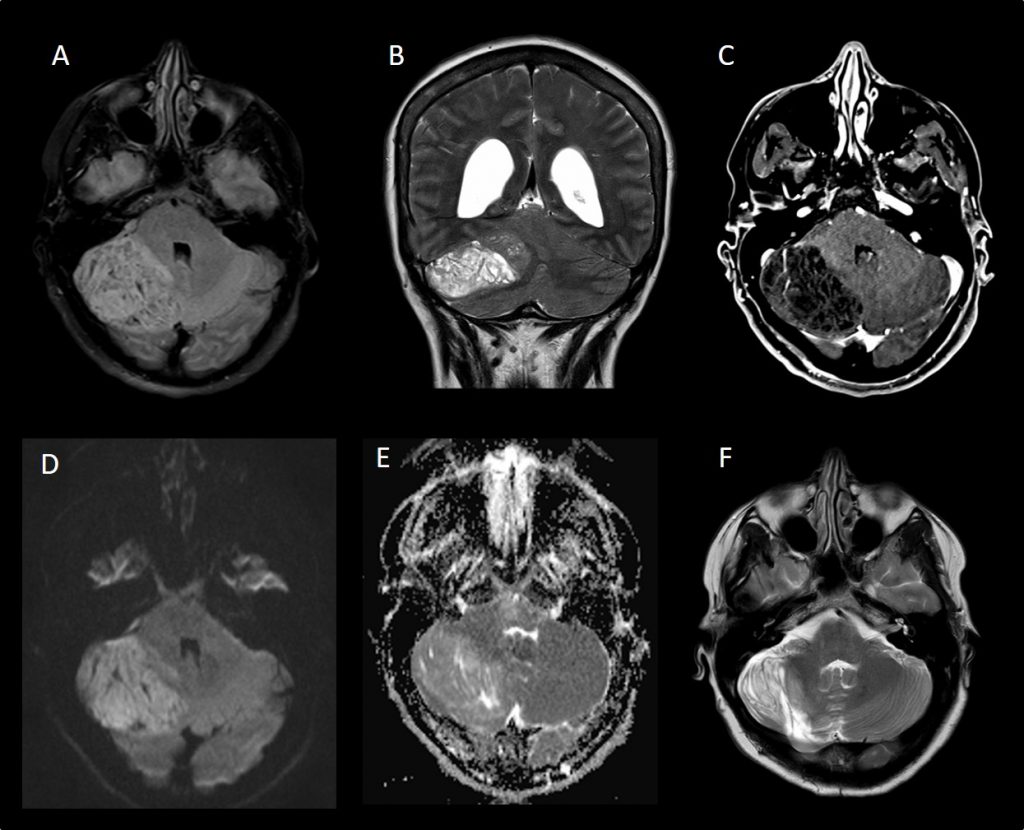
A: FLAIR axial . B: T2 coronal C: T1 con contraste. D: Difusión. E: Mapa de ADC. Se observa lesión expansiva y compresiva cerebelosa derecha, heterogénea con área lineales de hiper/hipointensidad, sin realce tras la administración de contraste, excepto algún vaso y con escasa restricción de la difusión. F: T2 axial post-quirúrgico.»
Diagnóstico
Diagnóstico Radiológico:
Enfermedad de Lhermitte Duclós asociado a síndrome de Cowden.
RESUMEN:
-
Se trata de una paciente que es diagnosticada a los 38 años de carcinoma de endometrio y posterior a un año de carcinoma de mama, se diagnostica de portadora de la enfermedad de Cowden (EC) y que posterior a episodios migrañosos se le realiza RM dando el diagnóstico de enfermedad de Lhermitte Duclós (LD)
- El gangliocitoma displásico cerebeloso o enfermedad de LD es un proceso expansivo de la fosa posterior, unilateral y de lento crecimiento. Clínicamente se hace evidente durante la 2.a y la 3.a década de la vida, no muestra predilección por género y puede estar asociado a diversas anomalías del desarrollo. Las evidencias clínicas y su estrecha vinculación con la EC (complejo hamartoma-neoplasia múltiple) hablan a favor de un origen hamartomatoso. La RM es el método de elección para el diagnóstico, revelando una masa cerebelosa sin realce con el contraste, hipointensa en en T1 e hiperintensa en T2, con un patrón estriado de líneas paralelas en su superficie (también descrito como atigrado, característico de la lesión) compatible con engrosamientos foliares con estructuras venosas entre ellos.
- LA EC es un trastorno genético multisistémico, en el que se desarrollan múltiples hamartomas en tejidos derivados de las tres hojas embrionarias. Sus localizaciones más comunes son en piel, mucosas, mama, tiroides y útero. También conlleva un riesgo incrementado para cáncer, cuyas localización más frecuente es también tiroides, mama y endometrio. El 40% de los pacientes presentan enfermedad de LD. No tiene tratamiento, salvo estrechas revisiones médicas anuales y en el caso de LD cirugía descompresiva.
- Se debe realizar diagnóstico diferencial con infarto subagudo cerebeloso con efecto masa, con displasias cerebelosas no clasificadas o con complejos de esclerosis tuberosa.
BIBLIOGRAFÍA:
-
Klisch J, Juengling F, Spreer J, Koch D, Thiel T, Büchert M, et al. Lhermitte-Duclos disease: assessment with MR imaging, positron emission tomography, single-photon emission CT, and MR spectroscopy. AJNR Am J Neuroradiol. 2001;22:824-30.
-
Shinagare AB, Patil NK, Sorte SZ. Case 144: Dysplastic cerebellar gangliocytoma (Lhermitte-Duclos disease). Radiology. 2009;251: 298-303.
- Lara-Torres HR, Sandoval-Balanzario MA, Rodríguez-Cervantes J, Barroso-Rodríguez N, Gómez-Ramírez AM, Becerra-Lomelí MM. Enfermedad de Lhermitte-Duclos. Informe de un caso y revisión de la literatura. Bol Med Hosp Infant Mex. 2006;63:402-7